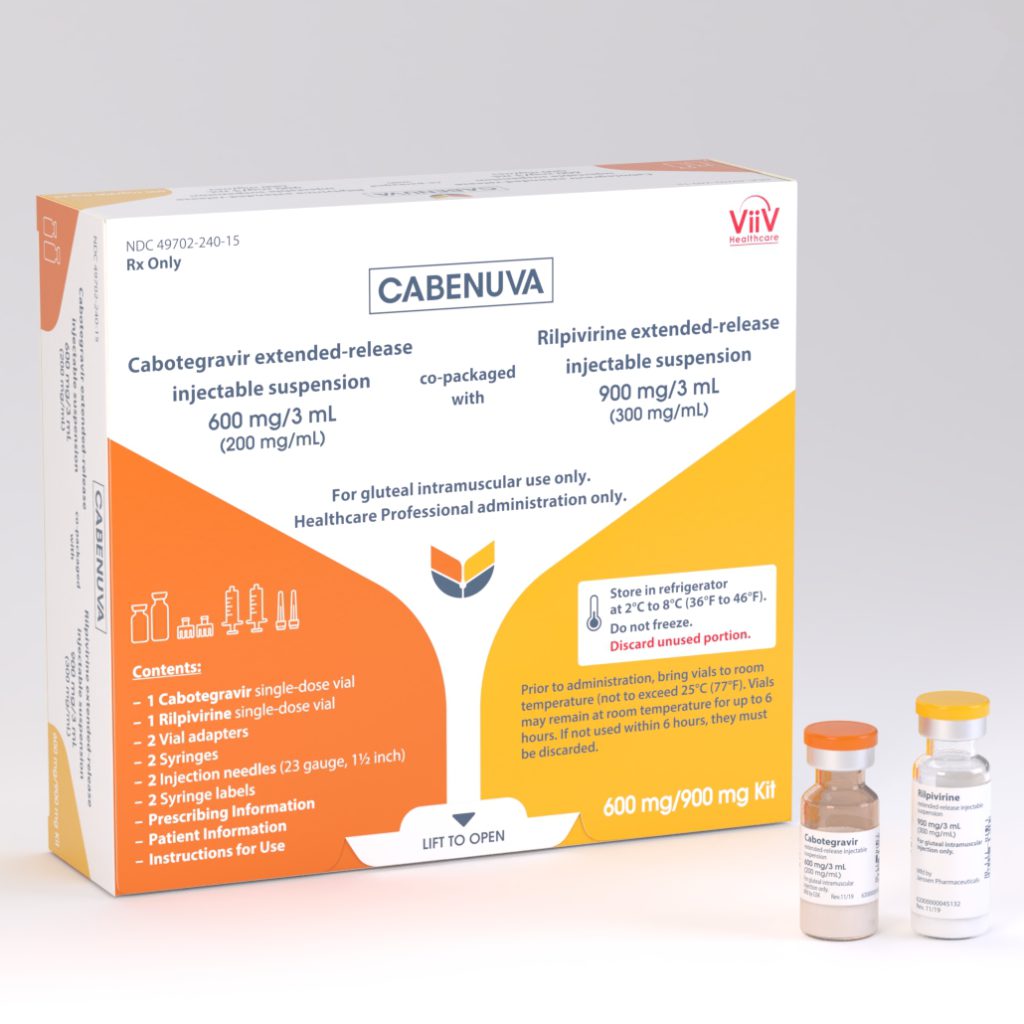
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило рилпивирин и каботегравир (Cabenuva) для двухмесячной дозировки для взрослых, живущих с ВИЧ.
Cabenuva была впервые одобрена FDA в январе 2021 года для введения один раз в месяц для лечения ВИЧ у взрослых с подавленным вирусом. Это лекарство было первым инъекционным полным антиретровирусным режимом, одобренным FDA.
Cabenuva может заменить существующее лечение у взрослых с подавленным вирусом на стабильный антиретровирусный режим при отсутствии истории неэффективности лечения и отсутствии известной или предполагаемой резистентности к рилпивирину и каботегравиру, говорится в пресс-релизе фармацевтических компаний Janssen, входящих в состав Johnson & Johnson. Cabenuva была разработана совместно Janssen и ViiV Healthcare.
Расширенное одобрение лейбла «знаменует собой важный шаг вперед в развитии лечения людей, живущих с ВИЧ», — заявила Кэндис Лонг, президент отдела инфекционных заболеваний и вакцин в Janssen Therapeutics, в пресс-релизе от 1 февраля. «С этой важной вехой у взрослых, живущих с ВИЧ, появился вариант лечения, который еще больше снижает частоту приема лекарств».
Это расширенное одобрение было основано на глобальном клиническом исследовании с участием 1045 взрослых с ВИЧ, которое показало, что прием Cabenuva каждые 8 недель (доза 3 мл каботегравира и рилпивирина) не уступает 4-недельному режиму (доза 2 мл обоих препаратов). На 48-й неделе исследования доля участников с вирусной нагрузкой выше 50 копий на миллилитр составила 1,7% в двухмесячной группе и 1,0% в одномесячной группе. Исследование показало, что показатели вирусологической супрессии были одинаковыми как для 1-месячного, так и для 2-месячного режима (93,5% и 94,3% соответственно).
Наиболее частыми побочными эффектами были реакции в месте инъекции, лихорадка, утомляемость, головная боль, скелетно-мышечная боль, тошнота, нарушения сна, головокружение и сыпь. Побочные реакции, о которых сообщалось у лиц, получавших лечение каждые 2 месяца или один раз в месяц, были схожими. Cabenuva противопоказан пациентам с реакцией гиперчувствительности на каботегравир или рилпивирин или тем, кто получает карбамазепин, окскарбазепин, фенобарбитал, фенитоин, рифабутин, рифампин, рифапентин, зверобой продырявленный и более одной дозы системного дексаметазона.
Источник:
https://www.medscape.com/viewarticle/967763?spon=1&uac=152429FG&impID=4004369&sso=true&faf=1&src=WNL_mdpls_220208_mscpedit_aids
